Conseil qualité

Découvrir
Certification ISO 19443 : Une norme essentielle pour la qualité et la sûreté nucléaire
L’ISO 19443 est une norme internationale dont la définition repose sur le management de la qualité et de la sûreté nucléaire, destinée aux fournisseurs et sous-traitants du secteur. Basée sur l’ISO 9001, elle intègre des exigences spécifiques pour les produits et services importants pour la sûreté nucléaire (IPSN), en complément des cadres réglementaires.
La norme ISO 19443 structure un système de management fondé sur des exigences renforcées (approche processus, amélioration continue, leadership) et aligné avec les référentiels internationaux comme ceux de l’AIEA. La certification ISO 19443 permet de maîtriser les risques, renforcer la traçabilité et répondre aux exigences des donneurs d’ordre.
Véritable levier d’accès au marché nucléaire, elle garantit la conformité aux exigences du secteur et positionne l’entreprise comme un acteur fiable et compétitif.
En savoir plus

Découvrir
Le Référentiel d’Evaluation des Etablissements et Services Sociaux et Médico-Sociaux (ESSMS)
Évaluation des ESSMS avec Préiso
Préiso, société française d’audit, de conseil et de formation, accompagne les établissements sociaux et médico-sociaux (ESSMS) dans l’évaluation de leur qualité et conformité. Nos experts travaillent selon le référentiel national d’évaluation, qui fixe les exigences à satisfaire selon le type de structure et le public accueilli.
Le référentiel comporte trois chapitres portant sur les personnes accompagnées, les professionnels et la gouvernance de l’ESSMS, répartis en neuf thématiques, de la bientraitance à la gestion des risques, et 157 critères évaluant 42 objectifs. Certains critères sont impératifs, nécessitant une action immédiate si non satisfaits.
Chaque critère est appliqué selon le secteur d’intervention, le type de structure et le type de public (personnes âgées, enfants, personnes en situation de handicap, protection de l’enfance, insertion…).
Préiso adapte son accompagnement aux spécificités de chaque ESSMS pour garantir une évaluation pertinente et personnalisée.
En savoir plus
Découvrir
Prestation
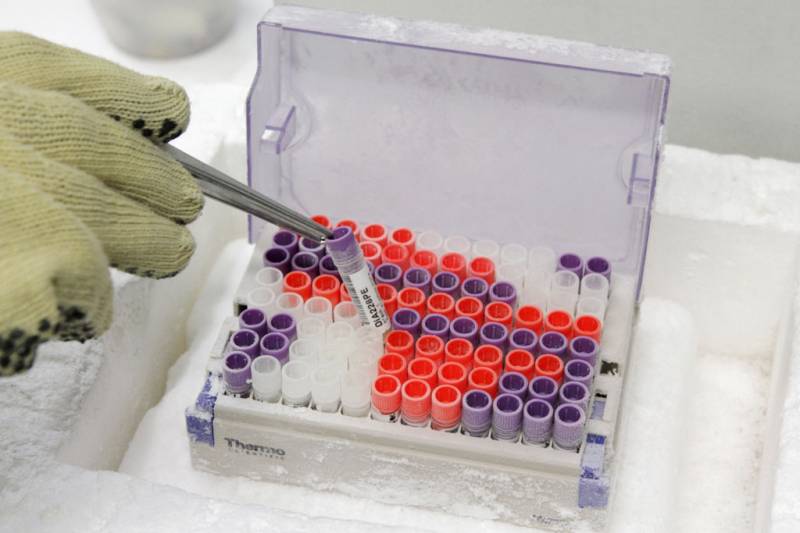
Norme ISO 20387 : Biotechnologie — «Biobanking» — Exigences générales relatives au «biobanking»
Certification ISO 20387 pour Centres de Ressources Biologiques (CRB)
Préiso accompagne les Centres de Ressources Biologiques (CRB) en France dans la mise en œuvre de la certification ISO 20387 Biotechnologie – Biobanking, garantissant la qualité et la fiabilité des ressources biologiques (tissus, cellules humaines et microbiennes) et des données associées pour la recherche et le développement.
La ISO 20387 est une démarche volontaire visant à :
Reconnaître la compétence et la fiabilité des biobanques auprès des acteurs de la recherche, du secteur pharmaceutique et de l’enseignement supérieur.
Intégrer un réseau de CRB certifiés par des organismes indépendants.
Prestations Préiso : état des lieux et faisabilité, accompagnement opérationnel, audits internes, formation, externalisation de la fonction de Responsable Qualité.
En savoir plus

L'ISO 22301 face aux scénarios de crise climatique
L’ISO 22301 est la norme internationale qui définit les exigences d’un Système de Management de la Continuité d’Activité (SMCA). Elle permet aux organisations, quel que soit leur secteur ou leur localisation, de planifier, mettre en œuvre et améliorer des dispositifs garantissant la reprise rapide des activités critiques face aux crises, pannes ou disruptions majeures.
La norme repose sur le cycle PDCA et inclut l’analyse d’impact (BIA), l’évaluation des risques physiques et liés à la transition climatique, ainsi que la prise en compte des parties prenantes. Depuis l’amendement 2024, les risques climatiques doivent être intégrés dans le SMCA, couvrant infrastructures, sécurité du personnel et chaînes d’approvisionnement.
L'ISO 22301 est la norme internationale de référence pour la continuité d'activité. Elle définit les exigences d'un Système de Management de la Continuité d'Activité (SMCA) et s'adresse à toutes les organisations, quel que soit leur secteur ou leur localisation.
Son objectif est clair : permettre à une organisation de se préparer, de réagir et de se remettre rapidement sur pied face à une crise, une panne ou toute perturbation majeure.
Structurée autour du cycle PDCA (Planifier – Déployer – Contrôler – Améliorer), la norme couvre plusieurs piliers essentiels : l'analyse d'impact sur les activités critiques (BIA), l'évaluation des risques — y compris physiques et climatiques — ainsi que la prise en compte des parties prenantes. Depuis l'amendement de 2024, les risques liés à la transition climatique font partie intégrante du SMCA, touchant aussi bien les infrastructures que la sécurité du personnel ou la solidité des chaînes d'approvisionnement.
Sur le plan opérationnel, l'ISO 22301 exige la formalisation de Plans de Continuité (PCA) et de Plans de Reprise d'Activité (PRA), régulièrement testés et évalués à l'aide d'indicateurs de performance (KPI).
Au-delà de la conformité, la norme représente un véritable levier stratégique : elle renforce la résilience de l'organisation, protège les collaborateurs, limite les interruptions d'activité et constitue un signal fort de fiabilité vis-à-vis des partenaires et clients.
En savoir plus

Découvrir
Norme ISO 13485 – les avantages du Marquage CE des dispositifs médicaux
ISO 13485 et marquage CE des dispositifs médicaux
Préiso, société française d’audit, conseil et formation, accompagne les fabricants et distributeurs de dispositifs médicaux dans le respect de la norme NF EN ISO 13485 et des exigences réglementaires du marquage CE.
Le marquage CE garantit la conformité des dispositifs médicaux aux normes techniques et la sécurité des patients, tout en permettant la libre circulation en Union européenne, sans présumer de l’origine du produit. Il s’appuie sur un Système de Management Qualité intégrant maîtrise des risques, suivi post-market, amélioration continue et contrôle des sous-traitants.
Avantages pour les organisations : reconnaissance client, fiabilité des produits, conformité réglementaire, maîtrise des risques et efficacité opérationnelle.
Préiso propose : accompagnement opérationnel ISO 13485, audit interne externalisé et formations dédiées aux dispositifs médicaux, avec des consultants experts : pharmaciens, responsables qualité et affaires réglementaires.
En savoir plus

Découvrir
Le Référentiel National Qualité : le référentiel d'application pour tous les prestataires de développement des compétences
Certification Qualiopi : ce qu’il faut savoir
Depuis la loi Avenir professionnel du 5 septembre 2018, tout organisme de formation souhaitant obtenir un financement public ou mutualisé doit être certifié Qualiopi. Initialement obligatoire au 1er janvier 2021, l’échéance a été repoussée au 1er janvier 2022 suite à l’ordonnance COVID‑19 du 1er avril 2020.
Le Référentiel National Qualité unifie et renforce les critères d’évaluation par rapport à Datadock : 7 critères (contre 6) et 32 indicateurs (contre 21), dont 10 spécifiques à l’apprentissage. Les organismes doivent désormais démontrer concrètement la qualité de leurs prestations, et non plus seulement la déclarer.
En savoir plus
Nous écrire
Les champs indiqués par un astérisque (*) sont obligatoires
Concrétisez votre projet


